Widma FT-IR
Widmo FT-IR rejestrowano w temperaturze 300 K w odległości 4000-500 cm-1 zakresy. Wynik pokazano na rysunku 1, a piki są bliskie 813 i 978 cm-1-1 Jest ustawiony na tryb NC. Szczyt znajduje się na wysokości 1253 cm-1 Jest to związane z wibracjami odkształcającymi N – C – H. Obserwuje się pasma 1410 i 1468 cm-1 Jest przypisany do CH3 sytuacja. Pasma są w pobliżu 2769 i 3058 cm-1 Jest to związane z trybem rozciągania C–H, a szczyt wynosi 3493 cm-1 Jest to tryb rozbudowy NH. Wynik ten jest w dobrej zgodzie z poprzednio raportowanymi wynikami [NH(CH3)3]2Kdkl423.
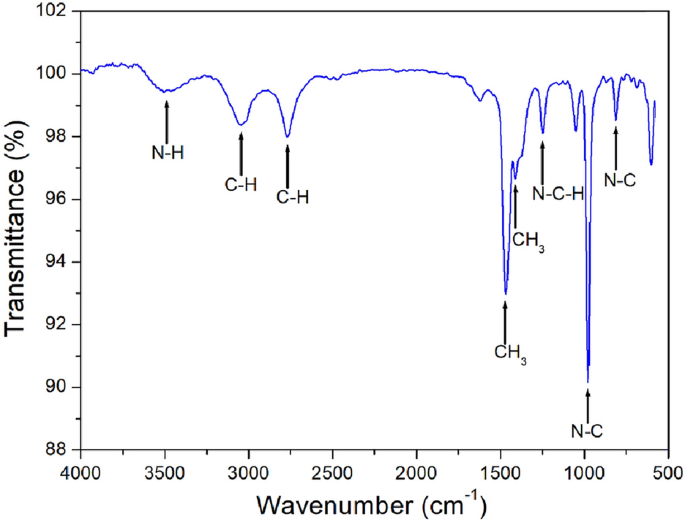
Widmo FT-IR [NH(CH3)3]2Chlorek cynku4 W temperaturze pokojowej.
Struktura krystaliczna
Wyniki XRD monokryształu [NH(CH3)3]2Chlorek cynku4 Wyhodowany tutaj kryształ otrzymano w temperaturze 300 K. Struktura monokrystaliczna ma układ rombowy z grupą przestrzenną Panamastałe sieci a = 10,6279(4) Å, b = 9,6297(4) Å, c = 14,9880(7) Å i Z = 4, co jest zgodne z wcześniej zgłoszonymi wynikami.19. Rysunek 2 przedstawia postać elipsoidy termicznej, liczbę atomową każdego atomu i dane XRD [NH(CH3)3]2Chlorek cynku4 Kryształy pokazano w tabeli 1. Nieskończone łańcuchy składają się ze sprzężonego ze sobą ZnCl4 Tetraedryczny i cztery podwójne mostki Cl– Jony związane z sąsiadującymi centrami cynku. Jak pokazano na rysunku 2, związek ten jest połączony trzema wiązaniami wodorowymi, N‒H···Cl, pomiędzy [NH(CH3)3] Kation f [ZnCl4] Anion. Długości wiązań Zn‒Cl, N‒C i N‒H···Cl oraz kąty wiązań Cl‒Zn‒Cl i N‒H···Cl przedstawiono w tabeli 2. Tutaj N‒H ···Cl wiązanie wodorowe składa się z kąta większego niż 120 stopni.
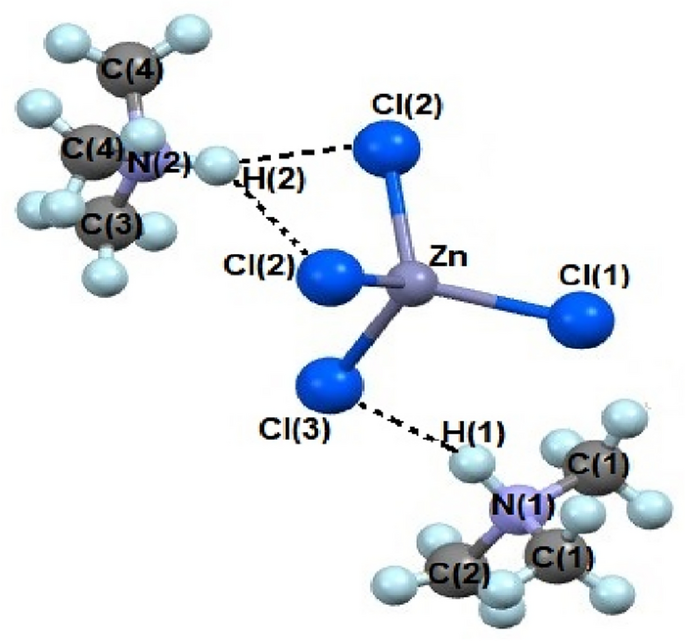
Struktura krystaliczna [NH(CH3)3]2Chlorek cynku4 Przy 300 tys.
Temperatury przejściowe
Termogram DSC proszku [NH(CH3)3]2Chlorek cynku4 Pomiaru dokonano w zakresie temperatur od 200 do 573 K przy szybkości ogrzewania 10°C/min. Rysunek 3 przedstawia cztery piki endotermiczne przy 257 K, 286 K, 326 K i 348 K. Silny pik endotermiczny uzyskano przy 553 K. Entalpie pięciu pików wynosiły odpowiednio 2,54, 7,99, 7,53, 1,86 i 17,58 kJ/mol. Zaczynając od 200 K, te pięć faz określa się jako fazę V poniżej 257 K, fazę IV pomiędzy 257 a 286 K, fazę III pomiędzy 286 a 326 K, fazę II pomiędzy 326 a 348 K i fazę I powyżej 348 K, jak pokazany na ryc. 3.
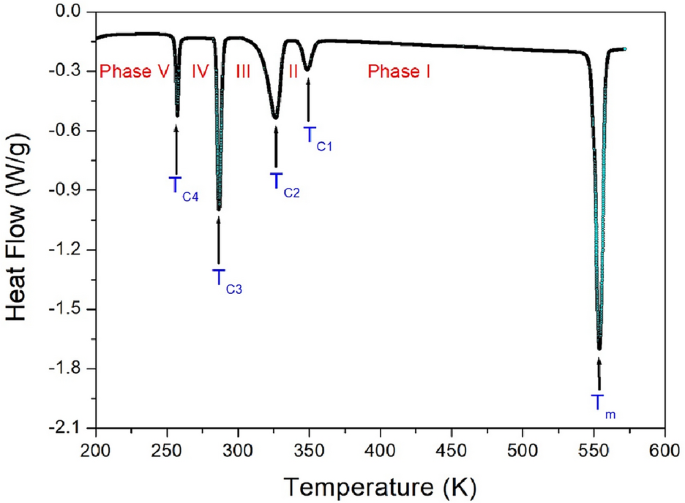
Krzywa różnicowej kalorymetrii skaningowej [NH(CH3)3]2Chlorek cynku4 Mierzono przy szybkości ogrzewania 10°C/min.
Aby dowiedzieć się, czy pięć pików endotermicznych pokazanych w wynikach DSC pokazanych na rysunku 3 to temperatury przejścia fazowego czy temperatura topnienia, zaobserwowano zmiany w pojedynczym krysztale za pomocą optycznego mikroskopu polaryzacyjnego wraz ze wzrostem temperatury. Dopóki temperatura nie wzrośnie do 530 K, monokryształ pozostaje prawie niezmieniony, ale monokryształ zaczyna się topić powyżej 550 K.
Dodatkowo mierzono eksperyment XRD proszkowy w zależności od zmiany temperatury. Wzory PXRD w zakresie 8°-50° (2θ) w różnych temperaturach przedstawiono na rysunku 4. Wzory PXRD poniżej 330 K (czarny) różnią się od zarejestrowanych powyżej 330 K (czerwony); Różnica ta jest związana ze strukturalnym przejściem fazowym w TC2 (= 326 K). Co więcej, wzory XRD zarejestrowane powyżej 330 K różnią się od tych zarejestrowanych przy 350 K (oliwka), a różnica ta jest związana z przejściem fazowym w TC1 (= 348 K). Wyniki te są zgodne z wynikami DSC. Teoretyczny wzór XRD przy 300 K pokazano na rysunku 4, który dobrze zgadza się ze wzorem eksperymentalnym.
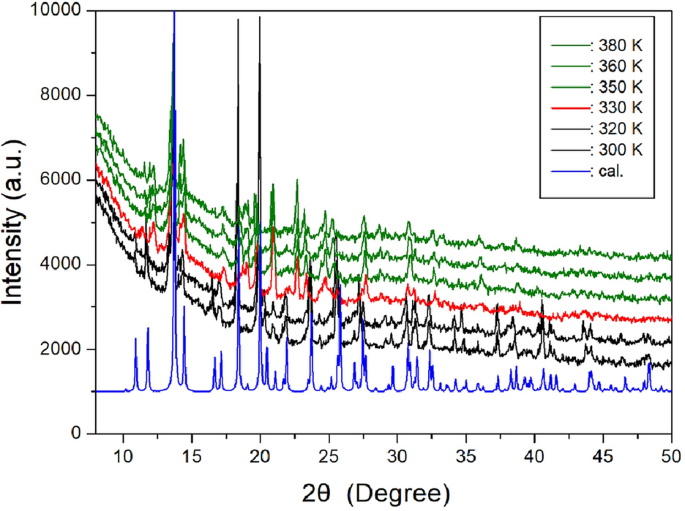
Wzory rentgenowskiej dyfrakcji proszkowej [NH(CH3)3]2Chlorek cynku4 W etapach III, II i I. Kolor niebieski to teoretyczny wzór proszku w temperaturze 300 K.
Temperatury przemian fazowych i temperatury topnienia pokazane przez PXRD i wyniki mikroskopii polaryzacyjnej dobrze zgadzają się z pikami endotermicznymi uzyskanymi na krzywej różnicowej kalorymetrii skaningowej (DSC). Na podstawie wyników DSC, PXRD i optycznej mikroskopii polaryzacyjnej określono temperatury przejścia fazowego jako TC4 = 257 K., TC3 = 286 K., TC2 = 326 K., TC1 = 348 K, a temperatura topnienia wynosiła TM = 553 tys.
Właściwości termiczne
Krzywe TGA pokazane na rysunku 5 uzyskano wraz ze wzrostem temperatury. Na krzywej TGA temperatura częściowego rozkładu Tdr Oznacza to ubytek masy wynoszący 2%, wynoszący 495 K, a materiał ten był stabilny termicznie do 495 K. [NH(CH3)3]2Chlorek cynku4 Kryształ wraz ze wzrostem temperatury nagle spadł z powodu częściowego rozkładu. Utratę masy cząsteczkowej obliczono jako 11% i 22% całkowitej masy cząsteczkowej poprzez częściową hydrolizę, odpowiednio, HCl i 2HCl. Początkowa utrata masy ciała (45%) występowała w zakresie 500-630 K. Z drugiej strony, na krzywej różnicowej analizy termicznej (DTA) pojawił się pik endotermiczny przy 342 K, który pojawia się jako różnicowa postać TGA, która była dobrze zgodna z temperaturą przemiany fazowej T.C1 Pojawia się w wyniku DSC. Ponadto stwierdzono, że całkowita utrata masy ciała następowała w temperaturach bliskich 800 K.
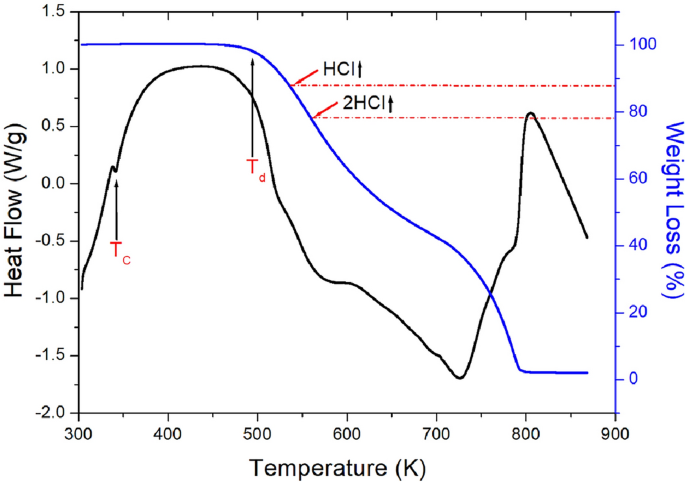
Krzywe TGA i TGA [NH(CH3)3]2Chlorek cynku4.
1oddać 13Przesunięcia chemiczne C MAS NMR
Przesunięcia chemiczne jądrowego rezonansu magnetycznego 1H w [NH(CH3)3]2Chlorek cynku4 Kryształy rejestrowano w etapach V, IV, III, II i I, jak pokazano na rycinie 6 1Widma H NMR NH i CH3 Uzyskane i ich wstęgi boczne 1Widmo H jest reprezentowane odpowiednio przez otwarte kółka i gwiazdki. Przy 300 tys. 1Zarejestrowano, że przesunięcie chemiczne H w NH wynosi około 7,78 ppm F 1H to przemiana chemiczna CH3 Otrzymano około 3,21 ppm. W zależności od zmiany temperatury, w pobliżu T nie następuje zmianaC4TC2CoC1ale nie 1H przesunięcie chemiczne NH w pobliżu TC3 Pojawia się zmiana. Jak pokazano na rysunku 6, 1Przekształcenia chemiczne H z CH3 Zamiast tego prawie nie zmienia się wraz z temperaturą 1Przesunięcia chemiczne H w NH ulegają zmianie, a wynik ten oznacza, że zmienia się geometria koordynacyjna 1H do CH3 Nie zmienia się w zależności od zmiany temperatury, podczas gdy geometria koordynacyjna jest w pobliżu 1H dla NH były zmianami.
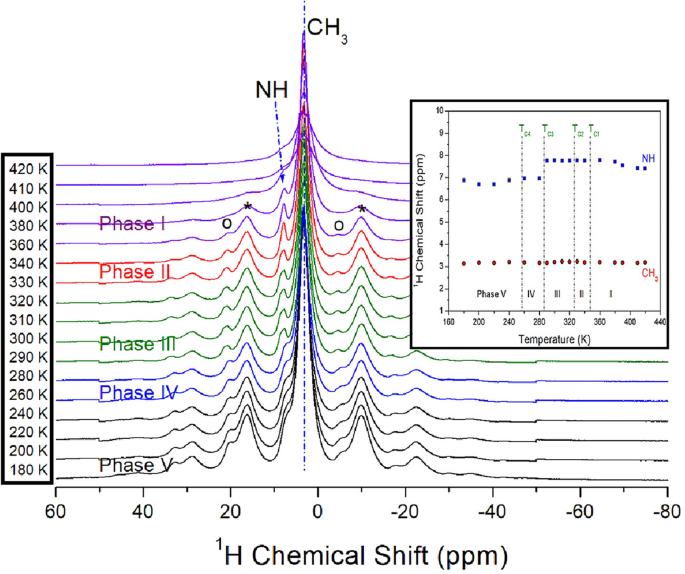
1H MAS NMR przesunięcia chemiczne NH i CH3 W [NH(CH3)3]2Chlorek cynku4 W etapach V, IV, III, II i I. Otwarte kółka oznaczają wstęgę boczną NH, a gwiazdki oznaczają wstęgę boczną CH3 (Wchodzić: 1H przemiany chemiczne NH i CH3 Temperatury zbliżone do przejścia fazowego).
the 13Przekształcenia chemiczne C NMR [NH(CH3)3]2Chlorek cynku4 Mierzono je w etapach V, IV, III, II i I wraz ze wzrostem temperatury, jak pokazano na ryc. 7. W strukturze krystalicznej pokazanej na ryc. 2, trzy 13Atomy C są połączone 1oddać 14N 13C Przemiany chemiczne CH3 Przy 220 K stopnia V pokazywał trzy sygnały (46,98, 46,24 i 45,87 ppm), a przy 300 K stopnia III (48,05 i 47,44 ppm) ulegał redukcji do dwóch sygnałów, a przy 420 K także ulegał redukcji do jednego sygnału pierwszy etap (47,89 ppm). pomimo 14n i 1H związał się wokół 13C w kationie i otaczającym środowisku 13C może się różnić w zależności od pobliskiego Cl–. To znaczy zmienić 13Przesunięcia chemiczne C nie są widoczne w pobliżu TC4podczas gdy zmiana przesunięcia chemicznego była znacząca u TC3. Dodatkowo uzyskano dwa sygnały pomiędzy TC3 CoC2i w temperaturze wyższej od TC1Uzyskano tylko jeden sygnał. Zmiana numeru 13Przekształcenia chemiczne C można wyjaśnić w następujący sposób. Oznacza to, że w piątym i czwartym etapie są trzy CH3 W różnych środowiskach, w trzecim i drugim etapie, istnieją dwa typy CH3 Z różnymi środowiskami. W szczególności w pierwszym etapie stwierdzono, że wszystkie otaczające środowiska 13bardzo łatwe3 Jesteśmy podobni. Liczba wierzchołków w 13Widma C NMR zmniejszają się wraz ze wzrostem temperatury, wskazując na wzrost symetrii koordynacyjnej wokół [NH(CH3)3] Jony dodatnie.
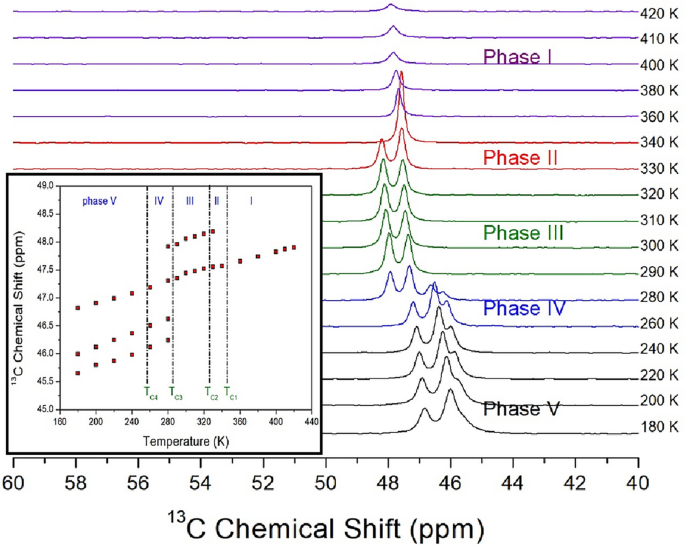
13Przesunięcia chemiczne C MAS NMR [NH(CH3)3]2Chlorek cynku4 W etapie piątym, czwartym, trzecim, drugim i drugim (wpisać: 13C Przemiany chemiczne CH3 W funkcji temperatury).
1oddać 13Czasy relaksacji wirowania sieci C NMR
Aby zrozumieć czas relaksacji sieci spinowej T1ρintensywność sygnału 1oddać 13Widma C NMR mierzono według różnych czasów opóźnienia. Krzywe zaniku wraz ze zmianą intensywności i czasów opóźnienia przedstawiono za pomocą poniższego równania38,39,40:
$$P\lewo( t \prawo) \, = \, P\lewo(0 \prawo)\exp ( – t/T_{1\rho } ),$$
(1)
gdzie q(R) to intensywność widma w czasie R A P(0) jest intensywnością widma w czasie R = 0.t1ρ Wartości dla 1oddać 13c w [NH(CH3)3]2Chlorek cynku4 Otrzymuje się go za pomocą równania. (1), a jego wyniki przedstawiono na rycinie 8 w etapach V, IV, III, II i I. 1oddać 13ct1ρ W etapach V i IV wzrasta wraz ze wzrostem temperatury i osiąga maksymalną wartość zbliżającą się do 300 K1ρ Wartości w pierwszym etapie wykazują tendencję do ponownego szybkiego spadku. Trend jest podobny w obu przypadkach 1oddać 13ct1ρ Wartości to oznaczają 1oddać 14wokół 13C związane i 13Atmosfera 14wokół 1H są ze sobą powiązane, więc uważa się, że wykonują te same ruchy. I fakt, że 13ct1ρ Wartość jest dłuższa niż 1HT1ρ Wartość oznacza transfer energii 1H związany do końca 13C. łatwe. W pobliżu TC1TC2CoC4T1ρ Wartości dla 1oddać 13C jest mniej więcej ciągłe, ale T1ρ Wartości bliskie TC3 Dokonuje się zmiany okresowej. Aby określić wielkość EA Na podstawie dynamiki molekularnej wyznaczono skalę logarytmiczną T1ρ Wartości dla 1000/T pokazano liniami ciągłymi na rysunku 8; HA Do 1H i stwierdzono, że w piątym i czwartym etapie wynosił 10,16 ± 0,88 kJ/mol. i EA Do 1H wynosił 37,08 ± 2,21 kJ/mol w pierwszej fazie. Z drugiej strony EA Do 13C otrzymane ze nachylenia T1ρ Natomiast odwrotna funkcja temperatury w fazach V i IV wyniosła 9,80 ± 0,45 i 9,83 ± 0,42 kJ/mol, natomiast dla 13C w pierwszej fazie wynosiło 45,04±1,99 kJ/mol 13C Przekształcenia chemiczne są nieco inne, EA W stopniach V i IV jest prawie taki sam w zakresie błędu. Warto zauważyć, że różnice w EA Jestem na etapie 5 i 4 i jestem bardzo stary.
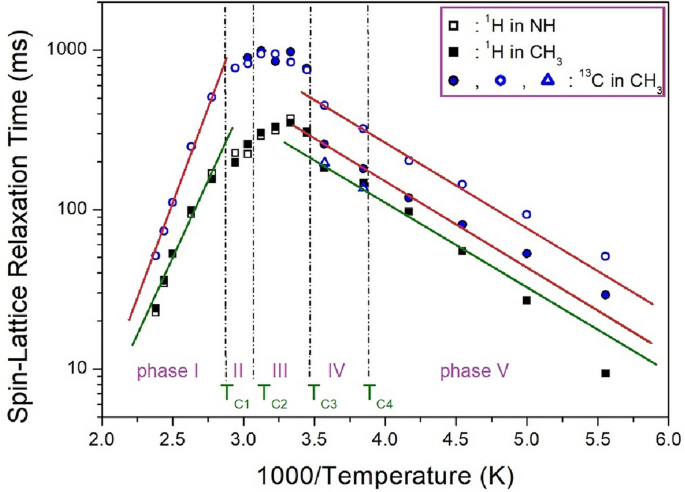
1oddać 13C NMR – czasy relaksacji sieci T1ρ W [NH(CH3)3]2Chlorek cynku4 W fazach V, IV, III, II i I. Nachylenia linii przedstawiają energie aktywacji przez T1ρ W funkcji odwrotnej temperatury.
the 1oddać 13ct1ρ Wartości wykazują tendencję do szybkiego wzrostu w piątym i czwartym etapie, natomiast szerokości te gwałtownie maleją w pierwszym etapie.1ρ W przypadku ruchów molekularnych typu Arrheniusa dzieli się je na części poruszające się szybko i wolno. Szybki ruch wyraża się jako ω1τC << 1, T1ρ-1~wyr(EA/KBT) i zwolnione tempo jako ω1τC >> 1, T1ρ~ω1-2 exp(-EA/KBT)38. Przy temperaturze około 300 K dzieli się ją na ruch szybki i zwolniony. the 1oddać 13ct1ρ Zamiast tego wartości w piątym i czwartym etapie były w trybie przyspieszonym 1oddać 13ct1ρ Wartości w pierwszym etapie przypisano reżimowi slow motion.

„Nieuleczalny myśliciel. Miłośnik jedzenia. Subtelnie czarujący badacz alkoholu. Zwolennik popkultury”.





![Struktury krystaliczne, przejścia fazowe, termodynamika i dynamika molekularna organicznych i nieorganicznych kryształów hybrydowych [NH(CH3)3]2ZnCl4 Struktury krystaliczne, przejścia fazowe, termodynamika i dynamika molekularna organicznych i nieorganicznych kryształów hybrydowych [NH(CH3)3]2ZnCl4](https://media.springernature.com/m685/springer-static/image/art:10.1038/s41598-024-53965-6/MediaObjects/41598_2024_53965_Fig1_HTML.png)
More Stories
Emdoor przygotowuje się do zaprezentowania swoich osiągnięć w zakresie nowej technologii sztucznej inteligencji podczas targów Global Sources Mobile Electronics Show 2024.
LinkedIn wykorzystuje Twoje dane do szkolenia Microsoft, OpenAI i jego modeli AI – oto jak to wyłączyć
Zapomnij o Apple Watch Series 10 — Apple Watch Ultra 2 w kolorze Satin Black to smartwatch, który warto mieć