Naukowcy pod kierunkiem laureata Nagrody Nobla Stefana Hilla z Instytutu Badań Medycznych im. Maxa Plancka w Heidelbergu opracowali mikroskop superrozdzielczy o rozdzielczości przestrzennej i czasowej jednego nanometra na milisekundę. Ulepszona wersja niedawno wprowadzonej mikroskopii MINFLUX o super rozdzielczości umożliwiła obserwację niewielkich ruchów pojedynczych białek z niespotykanym dotąd poziomem szczegółowości: krokowy ruch motorycznego białka kinezyny-1, gdy poruszało się wzdłuż mikrotubul podczas konsumpcji ATP. Praca została opublikowana w r naukipodkreśla moc MINFLUX jako rewolucyjnego nowego narzędzia do monitorowania zmian konformacyjnych w wielkości nanometrów w białkach.
Rozwikłanie wewnętrznego działania komórki wymaga znajomości biochemii poszczególnych białek. Mierzenie niewielkich zmian ich położenia i kształtu jest tutaj głównym wyzwaniem. Mikroskopia fluorescencyjna, w szczególności mikroskopia superrozdzielcza (tj. nanoskopia), staje się niezbędna w tej rozwijającej się dziedzinie. MINFLUX, wprowadzony niedawno system nanoskopii fluorescencyjnej, osiągnął już rozdzielczość przestrzenną od nanometra do kilku nanometrów — wielkości małych cząsteczek organicznych. Ale przeniesienie naszego zrozumienia fizjologii komórek molekularnych na wyższy poziom wymaga obserwacji z jeszcze wyższą rozdzielczością czasoprzestrzenną.
Kiedy grupa Stefana Hella po raz pierwszy wprowadziła MINFLUX w 2016 roku, był on używany do śledzenia fluorescencyjnie znakowanych białek w komórkach. Jednak ruchy te były przypadkowe, a śledzenie miało dokładność rzędu dziesiątek nanometrów. Ich badanie jest pierwszym, w którym zastosowano zdolność rozdzielczą MINFLUX do zmian konformacyjnych białek, w szczególności kinezyny-1 białka motorycznego. W tym celu naukowcy z Instytutu Badań Medycznych im. Maxa Plancka opracowali nową wersję MINFLUX do śledzenia pojedynczych cząsteczek fluorescencyjnych.
Wszystkie ustalone metody pomiaru dynamiki białek mają poważne ograniczenia, utrudniające ich zdolność do adresowania zakresu (sub)nm/(sub)milisekund. Niektóre zapewniają wysoką rozdzielczość przestrzenną, do kilku nanometrów, ale nie są w stanie śledzić zmian wystarczająco szybko. Inne mają wysoką rozdzielczość czasową, ale wymagają znakowania kulkami o 2 do 3 rzędów wielkości większymi niż badane białko. Ponieważ kulka tej wielkości prawdopodobnie zaburzy funkcjonowanie białka, badania z użyciem kulek pozostawiają otwarte pytania.
Fluorescencja pojedynczej cząsteczki
Jednak MINFLUX wymaga jedynie standardowej cząsteczki fluorescencyjnej o wielkości 1 nm jako markera wiążącego białka, dzięki czemu może zapewnić rozdzielczość i minimalną inwazyjność potrzebną do badania dynamiki białek natywnych. „Jednym z wyzwań jest zbudowanie mikroskopu MINFLUX, który działa blisko teoretycznego limitu i jest ekranowany przed hałasem otoczenia” — mówi dr Otto Wolf. uczeń w grupie. „Projektowanie sond, które nie wpływają na funkcje białek, ale ujawniają mechanizm biologiczny, to inna sprawa”, dodaje jego kolega Lukas Scheiderer.
Mikroskop MINFLUX, który wprowadzili naukowcy, może teraz rejestrować ruchy białek z rozdzielczością czasoprzestrzenną 1,7 nanometra na milisekundę. Detekcja wymaga jedynie około 20 fotonów emitowanych przez cząsteczkę fluorescencyjną. „Myślę, że otwieramy nowy rozdział w badaniu dynamiki poszczególnych białek i tego, jak zmieniają one kształt podczas pracy” – mówi Stefan Hill. „Połączenie wysokiej rozdzielczości przestrzennej i czasowej zapewnianej przez MINFLUX pozwoli naukowcom badać biomolekuły jak nigdy dotąd”.
Rozwiązanie stopniowego działania kinezyny-1 z ATP w warunkach fizjologicznych
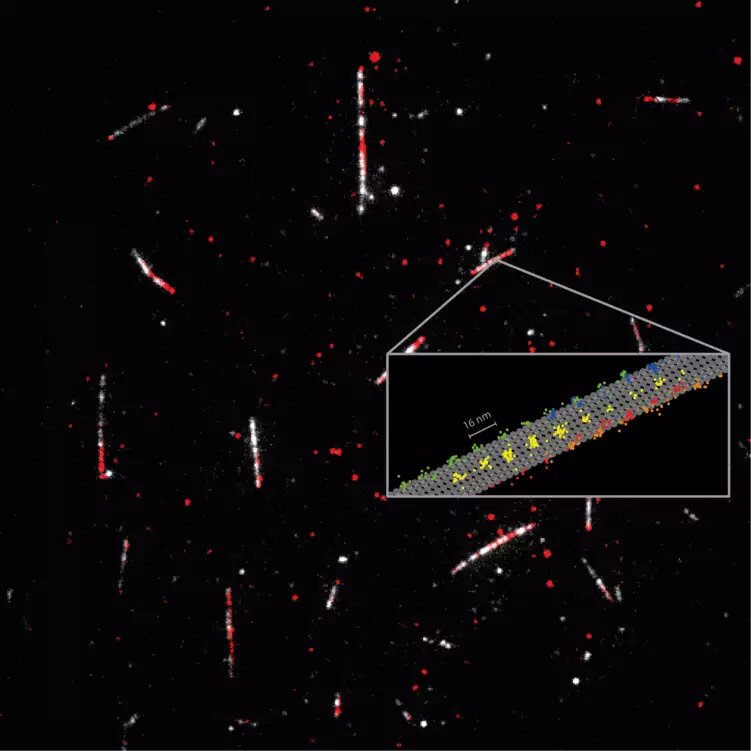
Kinezyna-1 odgrywa kluczową rolę w transporcie ładunku przez nasze komórki, a mutacje białek leżą u podstaw wielu chorób. W rzeczywistości kinezyna 1 „chodzi” wzdłuż włókien (mikrotubul), które rozciągają się nad naszymi komórkami jak sieć ulic. Ruch można sobie wyobrazić dosłownie jako „stąpanie”, ponieważ białko ma dwie „główki”, które naprzemiennie zmieniają swoje położenie na mikrotubulach. Ruch ten zwykle zachodzi wzdłuż jednego z 13 pierwotnych włókien tworzących mikrotubule i jest napędzany rozkładem głównego źródła energii komórki, ATP (trójfosforanu adenozyny).
Używając tylko jednego fluoroforu do znakowania kinezyny-1, naukowcy zarejestrowali normalne kroki 16 nm dla poszczególnych głów plus 8 nm, z rozdzielczością czasoprzestrzenną nanometr/milisekundę. Ich odkrycia wykazały, że ATP jest wchłaniany podczas przyczepiania jednej główki do mikrotubul, ale hydroliza ATP zachodzi, gdy obie główki są związane. Ujawniono również, że krok ten obejmuje obrót „łodygi” białka, która jest częścią cząsteczki kinezyny przenoszącej ładunek. Rozdzielczość czasoprzestrzenna MINFLUX ujawniła również rotację głowy na początkowym etapie każdego kroku. Co ciekawe, wyniki te uzyskano przy użyciu fizjologicznych stężeń ATP, co nie było jeszcze możliwe przy użyciu mikroznaczników fluorescencyjnych.
„Nie mogę się doczekać, aby zobaczyć, dokąd zaprowadzi nas MINFLUX. Dodaje nowy wymiar do badań nad działaniem białek. Może to pomóc nam zrozumieć mechanizmy stojące za wieloma chorobami i ostatecznie przyczynić się do opracowania metod leczenia”, dodaje Jessica Mathias, naukowiec ze stopniem doktora, który był wcześniej w grupie Hell, która obecnie bada zastosowania MINFLUX w różnych biologicznych kwestiach.
więcej informacji:
Jan Wolf i wsp., MINFLUX wyjaśniający nieskrępowany chód kinezyny-1, Nauki (2023). DOI: 10.1126/science.ade2650. www.science.org/doi/10.1126/science.ade2650

„Nieuleczalny myśliciel. Miłośnik jedzenia. Subtelnie czarujący badacz alkoholu. Zwolennik popkultury”.





More Stories
Emdoor przygotowuje się do zaprezentowania swoich osiągnięć w zakresie nowej technologii sztucznej inteligencji podczas targów Global Sources Mobile Electronics Show 2024.
LinkedIn wykorzystuje Twoje dane do szkolenia Microsoft, OpenAI i jego modeli AI – oto jak to wyłączyć
Zapomnij o Apple Watch Series 10 — Apple Watch Ultra 2 w kolorze Satin Black to smartwatch, który warto mieć